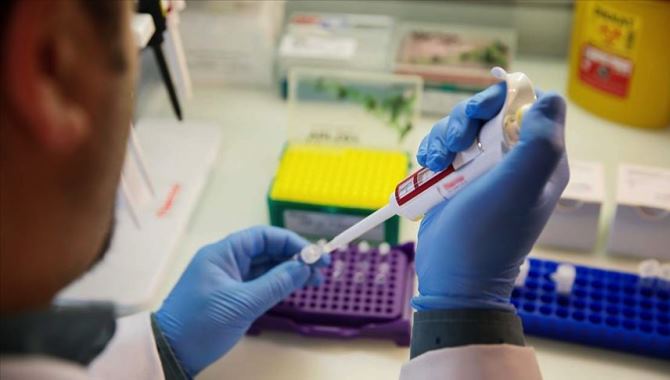
Tıbbi tanı kitlerinin ithalatında, gümrük idarelerince, Türkiye İlaç ve Tıbbi Cihaz Kurumunun fiziksel veya elektronik ortamda düzenleyeceği uygunluk yazısı talep edilecek.
Ticaret Bakanlığının Tıbbi Tanı Kitlerinin İthaline İlişkin Tebliğ'i Resmi Gazete'de yayımlanarak yürürlüğe girdi.
Tebliğ ile belirlenen tıbbi tanı kitlerinin ithalatında düzenlemeye gidildi.
Buna göre, tebliğle belirtilen tıbbi tanı kitlerinin insanlar için kullanılan türlerinde, Serbest Dolaşıma Giriş Rejimi veya Geçici İthalat Rejimi'ne ilişkin gümrük beyannamelerinin tescilinde, gümrük idarelerince, Türkiye İlaç ve Tıbbi Cihaz Kurumunun fiziksel veya elektronik ortamda düzenleyeceği uygunluk yazısı aranacak.
Söz konusu tanı kitleri, ilgili gümrük tarife pozisyonunda, "Bir mesnet üzerinde bulunan laboratuvarlarda veya teşhiste kullanılan reaktifler, bir mesnet üzerinde olsun olmasın laboratuvarlarda veya teşhiste kullanılan müstahzar reaktifler, standart maddeleri" ile "Dozlandırılmış veya perakende satışa uygun şekilde ambalajlanmış/hazırlanmış bağışıklık ürünleri" olarak tanımlandı.
Sağlık Bakanlığı tarafından yetkilendirilen firmalar için bu hükümler uygulanmayacak.
Tıbbi Cihazların İthalat Denetimi Tebliği kapsamında yapılacak başvurular, bu tebliğde yer alan eşya için uygunluk yazısı alındıktan sonra yapılacak.
Tebliğden önce tescil edilmiş beyannamelere, getirilen bu hükümler uygulanmayacak.
Tıbbi Tanı Kitlerinin İthaline İlişkin Tebliğ (İthalat: 2020/19)